医学撰写
我们为您提供高质量文件,以确保监管机构、公告机构或出版机构审查成功。
临床和法规医学攥写
成功的法规递交关键在于管理团队的技术专长。我们的医学撰写专家不仅拥有所需的医疗器械法规和临床专业知识,而且在众多的医疗和治疗领域拥有多年的临床实践经验。
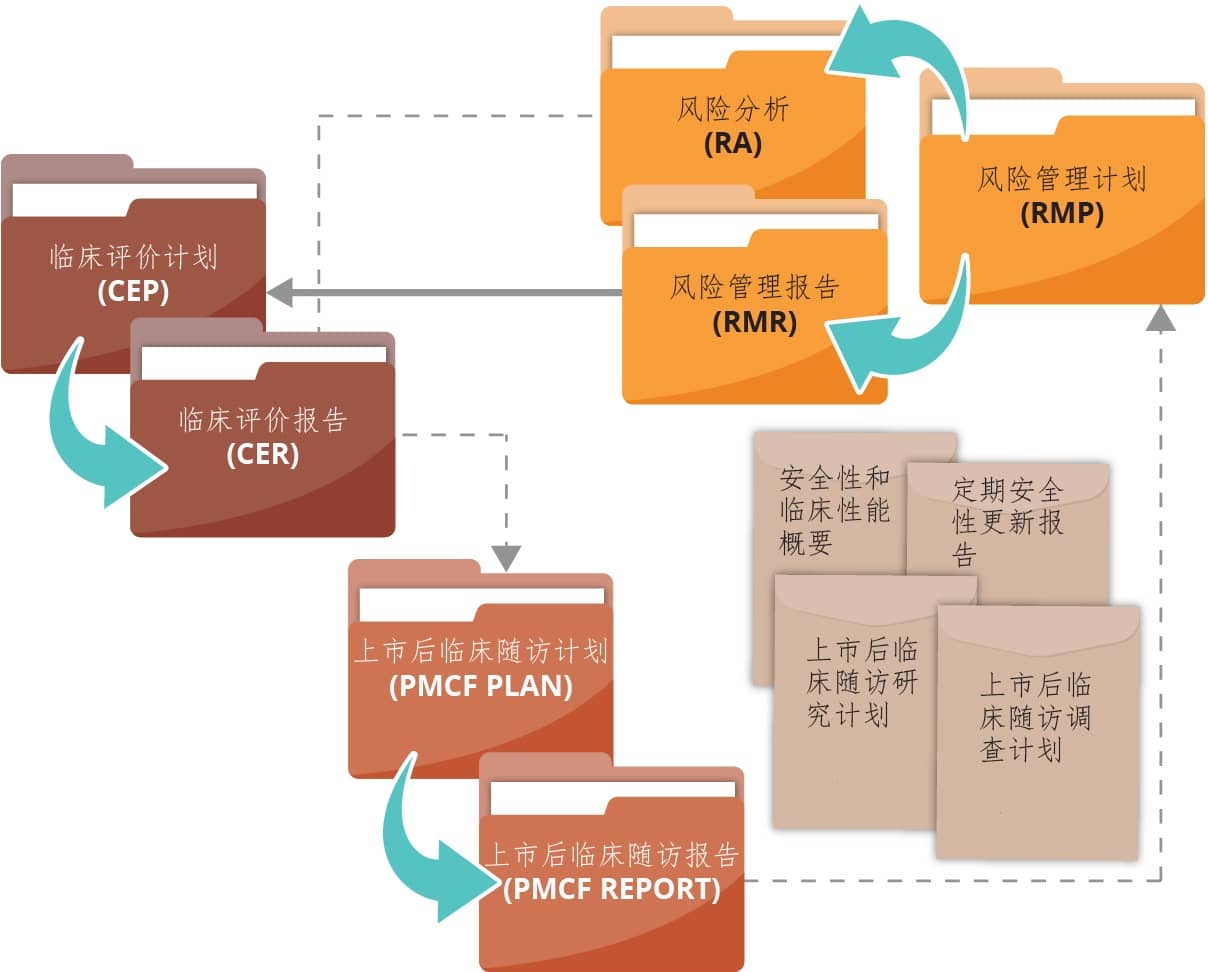
从法规角度,临床评价计划和临床评价报告需要阐述相关的临床证据,供其医疗器械上市或保持其持续市场销售。我们经验丰富的法规撰写专业人员有能力提供有效且合规的文件,供制造商递交公告机构。 拥有数百份临床试验方案和临床试验报告的撰写经验,我们还可以提供您的器械上市后随访的临床试验设计和文件撰写服务。
我们可以
- 定义/完善产品声称,建立有效的临床评价流程,确保产品成功上市或维持CE认证。
- 从MDD 到MDR的成功过渡
- 通过认真的规划和准备临床评价流程,满足CE认证的期限。
- 根据临床评价的发现,定义可行的上市后策略。
- 制定切实可行的临床研发计划用于支持制造商的临床试验方案/未来全球战略。
- 循序渐进,与客户共同验证,避免任何的误解,提高工作效率。
临床证据/临床评价:您的流程对了吗?
我们帮助您以正确的方式获取信息,生成有意义且合规的临床证据报告。
 联系我们获取1小时的免费咨询服务
联系我们获取1小时的免费咨询服务
